來源:CDE 發布時間:2015-12-22 浏覽量:1598

關于征求《臨床急需兒童用藥申請優先審評審批品種評定的基本原則》
意見與公示首批拟優先審評品種的通知
為貫徹落實國家食品藥品監督管理總局《關于藥品注冊審評審批若幹政策的公告》(2015年第230号)要求,我中心組織專家起草了《臨床急需兒童用藥申請優先審評審批品種評定的基本原則》,并根據上述原則對企業提出的兒童用藥優先審評申請進行了評定,現予以公示,以廣泛聽取意見和建議。對公示品種有異議的,請在2015年12月28日之前向我中心提交書面意見,說明理由。
公示日期為:2015年12月21日-2015年12月28日。
聯系人:黃清竹:huangqzh@cde.org.cn
杜宏金:duhj@cde.org.cn
附件1:臨床急需兒童用藥申請優先審評審批品種評定的基本原則
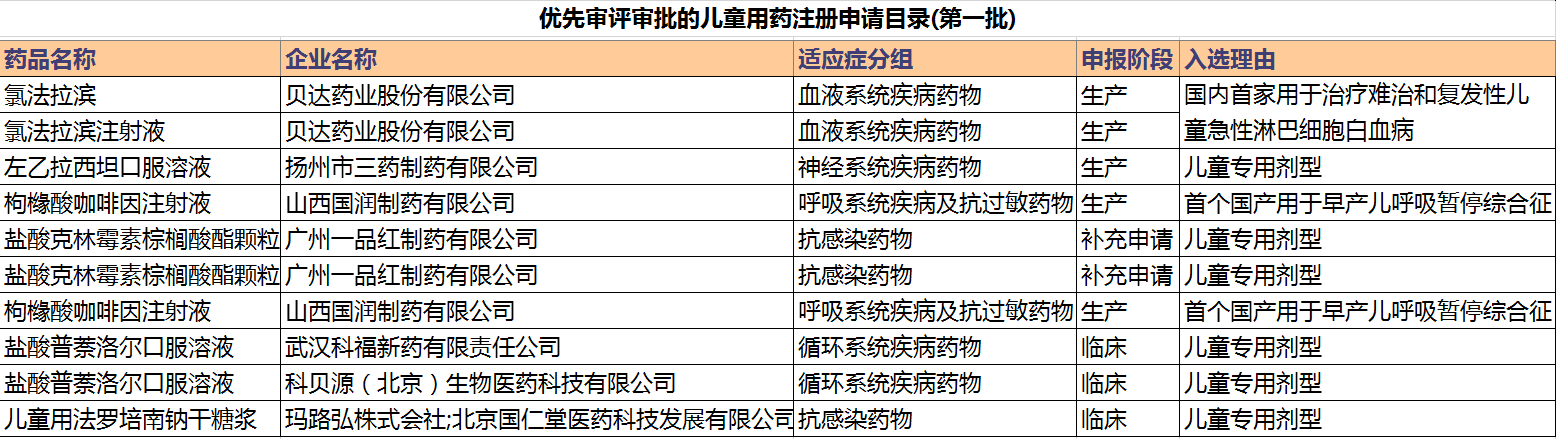
附件2:實行優先審評審批的兒童用藥注冊申請名單(第一批)
國家食品藥品監督管理總局藥品審評中心
2015年12月21日
臨床急需兒童用藥申請優先審評審批品種評定的基本原則
一、本原則适用于對臨床急需兒童用藥優先審評品種的 評定。
二、基本原則
(一)新藥申請:
此類申請,應滿足以下任一條件。
1、針對嚴重威脅兒童生命或者影響兒童生長發育,且目前無有效治療藥物或治療手段的疾病的申請;
2、相比現有的治療手段,具有明顯治療優勢的申請。
(二)改劑型或新增規格的申請:
此類申請應同時滿足以下兩個條件。
1、現有的藥品說明書中包含有确定的“兒童用法用量”的申請;
2、現行的劑型或規格均不适用于兒童,新增的劑型或規格适合于兒童的申請。
(三)仿制藥申請:
對于目前市場短缺的兒童用藥品,實行優先審評。仿制申報廠家的數目為多家申請的,按照申請先後排隊順序,對排第一位的優先審評,若經審評不符合要求,則取消優先資格,後面的同品種申請可按序增補替代。