


來源:廣州日報 發布時間:2015-12-25 浏覽量:1267
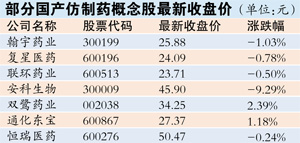
業内人士稱療效一緻性評價等新政提升藥品質量 有利龍頭股
廣州日報訊 今年醫藥行業整改不斷,大洗牌在所難免。就在如火如荼執行史上最嚴“藥物臨床試驗數據自查令”、導緻大批上市公司撤回新藥注冊申請之際,食藥監總局同時進行的還有仿制藥質量和療效一緻性評價,我國藥物市場上仿制藥聲勢最為浩大,但質量參差不齊。
業内人士認為,此舉将迫使部分仿制藥退市、有利龍頭股搶市場,而藥品總體質量與價格也可能同步提升。
仿制藥同質化嚴重
據了解,今年上半年我國醫藥制造業收入增速創15年來新低,增速僅8.76%,其中仿制藥聲勢依然浩大。中國化學制藥工業協會常務副會長潘廣成對外透露,中國藥企共擁有藥品批準文号18.7萬個,其中化學藥品批準文号12.1萬個,絕大部分為仿制藥;2014年化學藥品批準上市品種中,仿制藥220個,占47%。
“一方面,我國仿制藥總體呈現藥企衆多、産品同質化嚴重、價格厮殺激烈、質量普遍不高的現狀;另一方面,相較于化學仿制藥與國際原研藥的較大差距,反而基因測序、生物制藥産品取得了不小突破。”一位行業觀察人士表示。“有的仿制藥曾貢獻不小,但現在已跟不上時代需求。”其表示,在缺醫少藥年代,政策對待仿制藥較為寬松,但不少藥品質量有待提升。
部分仿制藥揮别市場
該公告指出,對2007年10月1日前批準的國家基本藥物目錄中化學藥品口服固體制劑,應在2018年底之前完成一緻性評價,到期未通過評價的,将注銷藥品批準文号;而對2007年以前批準上市的其他仿制藥品和2007年以後批準上市的仿制藥品,自首家品種通過一緻性評價後,其他生産企業的相同品種在3年内仍未通過評價的,也要注銷藥品批準文号。
公告指出,通過一緻性評價的品種,醫保支付予以支持,醫療機構優先采購并臨床優先選用。同一品種有3家以上通過一緻性評價時,集中采購時不再選用未通過評價的品種。
“這意味藥企面臨一場時間緊迫、名額有限的淘汰賽,而且費用不低。”廣東賽烽醫藥科技有限公司有關負責人表示,一緻性評價要求企業在申報時把所有流程走一遍,每個藥品都需要重新申請文号,耗時長且耗資多。“規模不大、資金有限的藥企受沖擊或較大,但現在可以進行評價外包。”有業内人士分析認為,仿制藥一緻性評價将大幅提升藥品質量,但藥價也可能稍有擡高。
對資本市場有何影響?觀察人士表示,資金實力雄厚、産品市場穩固的上市公司的決心較大,會抓緊進行評價,通過者甚至可能擠掉競争對手,進一步從市場獲益,所以一緻性評價或有利龍頭股。