


來源:新康界;白小空 醫藥市場的旁觀路人甲 發布時間:2016-01-18 浏覽量:1553
《藥品注冊管理辦法》2007年7月10日頒布,本文回顧2008年至2015年藥劑國産申報熱點的産品,從中可以看出國内研發熱點的改變。
| 2008年到2015年國産申報排名前十的産品
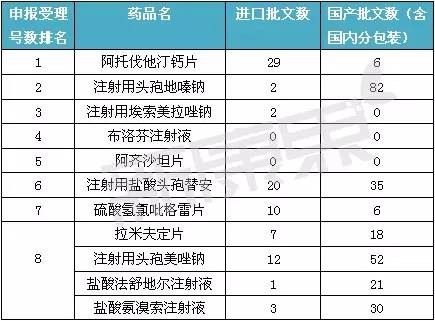
分析2008年到2015年國産申報排名前十的産品,可以将産品申報政策分為三類:
1)跟随策略:仿制國内已上市銷售額較大的原研産品
筆者通過鹹達數據V3.2發現,阿托伐他汀鈣片是2008年以來國産廠家申報最多的藥品,國産申報的受理号數雖多,但是實際上真正國産廠家(不含分包裝)的批文隻有2家,分别為北京嘉林藥業股份有限公司和浙江新東港藥業股份有限公司,這或許和阿托伐他汀鈣片專利有關。同樣受限于專利但申報量較多的還有排名第三的注射用埃索美拉唑鈉,目前還沒有一家仿制藥獲批。
2)簡單重複:抗生素政策限制了三年才影響到研發申報
注射用頭孢地嗪鈉、注射用鹽酸頭孢替安和注射用頭孢美唑鈉分别排在第二、第六和第九,在2011年抗生素管理條例頒布後直到2013年,抗生素針劑幾乎每年都有産品在前十。由此可見從政策監管到市場反應再到研發方向改變,有一定時間差。
3)搶仿:國外已上市國内沒上市的産品先搶為赢
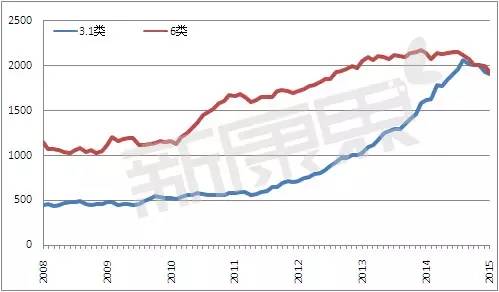
布洛芬注射液和阿齊沙坦片就屬于國外已上市國内沒上市的産品,此類産品一般選擇國内已上市市場規模較大的通用名産品改劑型。筆者整理2008年至2015年各月年積累申報量發現,除了2015年9月,3.1類年累計申報量幾乎都低于6類年累計申報量。整體趨勢而言,3.1類和6類的申報數量都在增加,其中2011年6類年累計申報增量高于3.1類,2012年和2013年3.1類和6類增量基本持平,2014年和2015年3.1類的申報增量高于6類。這意味着近兩年國内搶仿申報數量越來越多且“搶仿”已成為研發項目申報的熱點選擇。
2008年至2015年年累計申報量:3.1類vs 6類
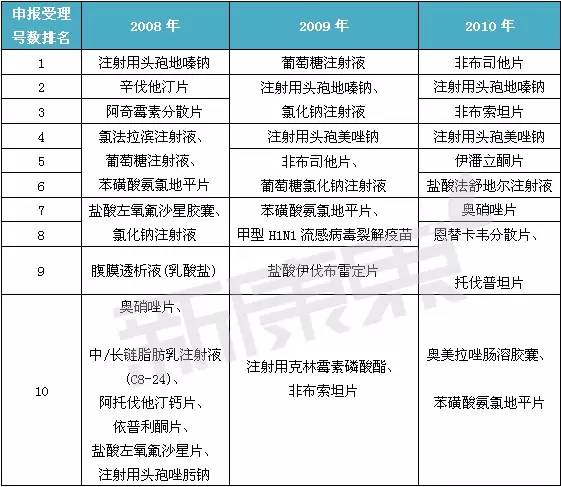
| 2008年至2015年曆年國産申報排名前十的産品
2008年至2009年,抗生素類針劑和片劑如注射用頭孢地嗪鈉、阿奇黴素分散片、注射用頭孢美唑鈉和鹽酸左氧氟沙星膠囊,心血管口服藥如辛伐他汀片和苯磺酸氨氯地平片,輸液如葡萄糖注射液和氯化鈉注射液都是申報熱點。2014年以後抗生素針劑和片劑已無産品排進前十,輸液類更是在2010年以後沒有産品進入前十。心血管類産品則始終有産品上榜。這從側面反映了當藥品使用往規範化方向發展的時候,産品申報同樣也會往治療用藥物方向靠攏,依靠政策和利潤驅動的産品能風光一時,但未必能長期利好。
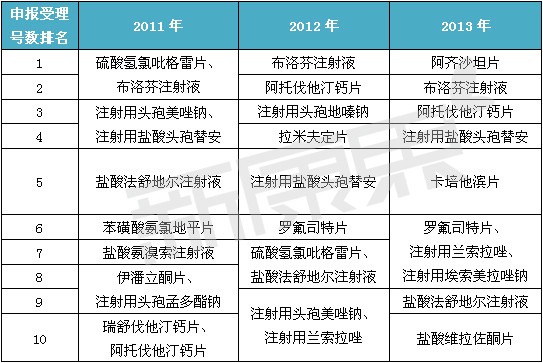
仿制國内已上市産品方面,專科用藥一直是申報熱點:2011年的申報最熱點為硫酸氫氯吡格雷片,2014年則為注射用埃索美拉唑鈉。申報的治療領域也呈現多元化:腫瘤藥如卡培他濱片和達沙替尼片,男性勃起功能障礙藥如他達拉非片,非甾體抗炎鎮痛藥如塞來昔布膠囊都是研發申報的新興熱點領域。
除了2014年,2010年至2015年都有國内未上市國外已上市的搶仿産品排在申報受理号數量第一位。2010年受理号數最多的是非布司他片,申報類型是3.1類,目前生産批文有6個,都是2013年獲批的,對應廠家3家。2011年和2012年布洛芬注射液排在第一位。2013年治療高血壓用藥阿齊沙坦片排第一。2015年成人重度抑郁障礙MDD藥氫溴酸沃替西汀片排第一位。
2008年至2010年申報前十名
2011年至2013年申報前十名
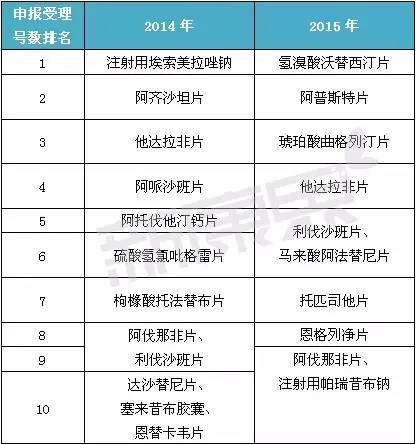
2014年至2015年申報前十名
| 小結
回顧2008年至2015年申報數據可得,我國研發申報項目越來越與國際接軌,立項越來越注重臨床必要性。2015年國内未上市國外已上市的仿制産品申報受理号數與國内已上市的仿制産品申報受理号數基本持平。2015年的注冊法規取消了國内未上市國外已上市的仿制産品的新藥證書,而且國家對仿制藥的要求提升到與原研藥一緻的水平,臨床審查從嚴,項目實施難度加大,項目立項将會越來越慎重。